|
Существует несколько систем, регулирующих
механизм эрекции:
- Центральная нервная система.
- Вегетативная нервная система.
- Не-адренергическая, не-холинергическая
система.
- Гормональная система.
Регулирующее
действие центральной нервной системы
схематично представлено на
схеме №1. Оно
реализуется через допаминергические
механизмы (центральные Д2
рецепторы), серотонин,
5-гидрокситриптамин, а также
окситоцин и адрснокортикотропный
гормон (АКТГ). Гормоны окситоцин и
АКТГ оказывают свое стимулирующее
действие на эрекцию только при
иньек-ции в определенные области
головного мозга. Избирательно эти
вещества в сексуальном обеспечении
не участвуют. Их действие зависит от
взаимодействия с другими факторами,
включая содержимое местной среды и
стероидных гонад, наряду с
дифференцированными воздействиями в
различных точках головного мозга
[1,14,17].
СХЕМА 1
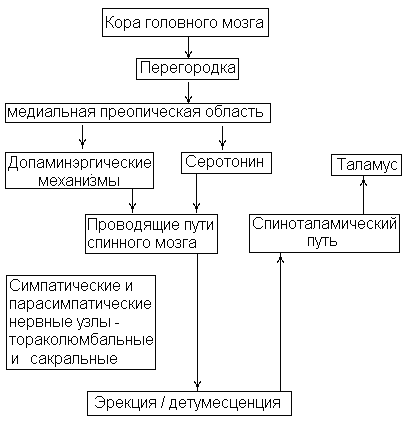
Вегетативная нервная система
реализует свой эффект через
холинергические и адренсргические
механизмы. На схеме №2
представлено регулирующее влияние
вегетативной нервной системы и
не-адренергической,
не-холенергической системы.
Холинергическим медиатором является
ацетилхолин (АХ). Многочисленными
исследованиями было доказано, что
парасимпатическая нервная система не
ин ет нервных окончаний на
гладкомышечных элемент кавернозной
ткани, а ацетилхолин не обладает
релакс рующим эффектом. Введение АХ
в аорту, в артерию п левого члена,
внутривенно не оказало эректогенно
действия. Действие парасимпатической
нервной сип мы основано на
блокировании констрикторного а фекта
симпатической нервной системы.
Определенно влияние
парасимпатическая нервная система
оказыкк также и на выделение
эндотелиальных факторов рела сации.
К этим факторам относятся
простагландин Е (PGE1) простациклин
[10, 19]. Подобно PGE1, проел циклин
- мощный вазодилятатор. Синтез
проста циклина стимулируется
мускариночувствительным агонистами.
Противоположным действием обладая
простагландин-Р2 (PG-F2), который
вызывает сокраще ние гладкомышечных
структур кавернозной ткани
Эндотелиальный слой лакун
кавернозной ткани имея синапсы
холинергической нервной системы. При
ста' муляции АХ эндотелиальные
клетки вырабатывают эн дотелиальный
фактор релаксации NO, способный ока
зывать релаксирующее воздействие на
подлежащи! гладкомышечный слой
[39,41].
Адренергические механизмы
реализуются через активацию или
блокирование альфа-адренорецепторов,
где нейромедиатором является
норадреналин (NA Интракавернозное
введение альфа-адреноблокаторо
(фентоламина) вызывает эрекцию.
Введение же альфа адреноагониста
(метараминол) способствует детумес
ценции. Ни бета-адреноблокатор
(пропранолол), ни
Схема 2
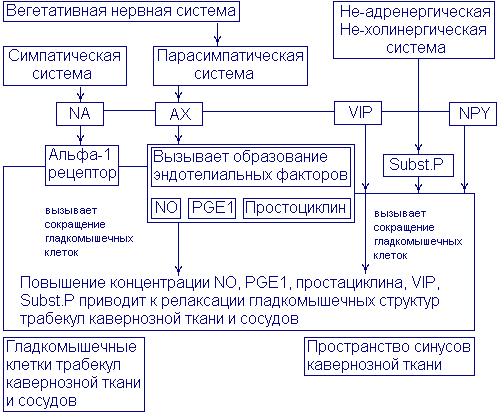
селективный альфа2-адреноблокатор
(идазоксан) не оказывают действия
при интракавернозном введении
(10,30, 38]. Эти данные заставляют
предполагать, что в покое тонус
трабскулярной гладкой мускулатуры
поддерживается постоянной альфа
1-адренорецепторной стимуляцией.
Однако бета-блокаторы, особенно
про-пранолол, способны вызвать
импотенцию. Механизм этого явления
не известен.
Не-адренергическая,
не-холенергическая система реализует
свой эффект через пептидергические
механизмы. Медиаторами этой системы
являются вазо-интестинальный пептид
(VIP), нейропептид Y (NPY),
субстанция Р (subst.P), кальцитонин
ген-связанный пептид (CGRP). VIP
представляет собой состоящий из 28
аминокислот пептид с мощным
сосудорасширяющим действием, который
действует через иммуноре-активные
волокна, иннервирующие артериальные,
артериолярные и несосудистые гладкие
мышцы кавернозной ткани. Подобно
VIP, subst.P оказывает
ре-лаксирующее действие на
кавернозную ткань, но обнаруживается
в меньших концентрациях. NPY
обладает противоположным действием -
прямым и опосредованным
сосудосуживающим. Ему отводится роль
в пенильной детумесценции.
Кальцитонин ген-связанный пептид
(CGRP) присутствует в нервных
окончаниях кавернозных тел. Механизм
действия заключается в индукции
аденилатциклазы, что приводит к
возрастанию концентрации ц-АМФ [1,
12, 29].
Регулирующее действие эндокринной
системы реализуется через влияние
тестостерона, его метаболитов,
пролактина на органы мишени [13,18].
У мужчин с нормально работающими
гонадами корреляции между уровнями
тестостерона и степенью сексуальной
заинтересованности, активности или
эректильной функцией отсутствует.
Дефицит тестостерона также не
приводит к поражению механизма
эрекции, а является патогенетическим
фактором снижения либидо. Получены
доказательства действия тестестерона
на активность бульбокавернозных
мышц. Пролактин - гормон передней
доли гипофиза принимает участие в
регуляции эрекции. У мужчин,
страдающих аденомой гипофиза,
отмечалась гиперпролактинемия, что
приводило к развитию эректильной
дисфункции [1б]. После купирования
гиперпролактинемии эректильная
функция быстро восстанавливалась.
Клеточные механизмы эрекции
На клеточном уровне раслабление
гладкомышечных клеток медиируется
двумя различными механизмами (схема
№3), взаимодействующими друг с
другом: ц-АМФ и ц-ГМФ. Повышение
внутриклеточной концентрации данных
вторичных передатчиков (ц-АМФ и
ц-ГМФ) приводит к активации
протеинкиназы, под воздействием
которой происходит фосфорилирова-ние
белков клеточной мембраны,
активирующее вольтаж-зависимые
кальциевые каналы, что завершается
выходом кальция во внеклеточное
пространство. Снижение концентрации
Са во внутриклеточном и повышение
его концентрации во внеклеточном
пространстве приводит к изменению
потенциала клеточной мембраны и
релаксации гладкомышечных клеток
тра-бекул кавернозной ткани и
эрекции пениса.
Схема 3
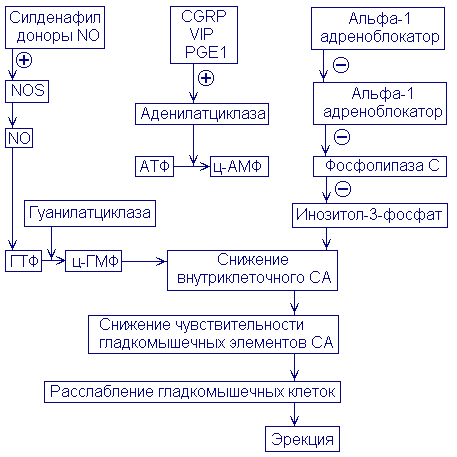
Адренергическая система обладает
эректолитическим действием.
Норадреналин, выбрасываемый из
нервных окончаний, воздействует на
постсиптические
альфа-1-адренорецепторы, провоцируя
сокращение гладкомышечных клеток
кавернозных тел и, вследствие этого,
де-туменисценцию. Основной эффект
реализуется через постсинаптические
альфа-1-адренорецепторы, однако
велика роль и пресинаптических
альфа-2-адреноре-цепторов,
запускающих механизм отрицательной
обратной связи [19, 38]. При
возрастании концентрации
норадреналина в синаптической щели
активация аль-фа-2-постсинаптических
рецепторов блокирует дальнейший
выброс. В этой связи видится
перспективным использование
селективных альфа-1
адреноблокато-ров, т. к
неселективные (фентоламин), блокируя
и альфа-1, и
альфа-2-адренорецепторы, выключают
механизм отрицательной обратной
связи. В результате концентрация
норадреналина в синаптической щели
безудержно повышается и происходит
частичное вытеснение препарата с
рецепторов [27,32].
По месту воздействия
адреноблокаторы можно разделить на
центральные, которые действуют
преимущественно на уровне головного
и спинного мозга, и периферические,
блокирующие эффект уже
выбросившегося норадреналина в
тканях.
Препараты центрального действия
на эрекцию
Йохимбин
Наиболее известный и
исследованный препарат этой группы.
Являясь алкалоидом раувольфии,
блокирует альфа-2 рецепторы
центральной локализации. Это
приводит к возрастанию концентрации
норадреналина в некоторых областях
головного мозга, что повышает либидо
и, опосредованно, улучшает потенцию.
Прямого действия на эрекцию нет. Т.
о. может применяться, в основном,
при психогенной ЭД 3, 22). В высоких
концентрациях йохимбин может
блокировать также серотониновые,
допаминовые и гистаминовые
рецепторы, что обусловливает
развитие толерантности к препарату.
Проводившимися исследованиями не
удалось выявить достоверную разницу
между йохимбином и плацебо при
лечении ЭД [20,23].
Побочные эффекты включают
беспокойство, тошноту, сердцебиение,
тремор и повышение диастолического
АД.
Для преодоления толерантности и
повышения эффективности разработаны
новые селективные центральные
альфа-2-адреноблокаторы идазоксан
иэфарок-сан, однако по
стимулирующему эффекту на эрекцию
они мало превосходят йохимбин [28].
Делаквамин
Новый препарат, в 100 раз более
селективный к альфа-1,чем к альфа-2
рецепторам, чем йохимбин, но в
ранних клинических исследованиях его
эффект мало превосходит эффект
плацебо [10, 22].
Препараты периферического
действия на эрекцию
Фенталамин
Фентоламин обладает
приблизительно равным сродством к
альфа-1 и альфа-2 адренорецепторам
периферических тканей. Эрекция,
возникающая при вну-трикавернозном
введении фентоламина, отличается
меньшей ригидностью, чем при
введении селективных альфа-1
адреноблокаторов [30, 38]. Это
связано с отключением механизма
отрицательной обратной связи,
описанным выше. Т. о. фентоламин
увеличивает транскорпоральный
кровоток, при этом достоверно не
увеличивая внутрикавернозное
давление. Учитывая недостаточное
качество эрекции при монотерапии, в
настоящее время в основном
используется в виде комбинаций (с
папаверином, PGE1, VIP).
Недавно разработана оральная и
буккальная форма фентоламина
(Вазомакс), которая изучалась в
двойном слепом плацебоконтролируемом
исследовании на 700 пациентах [30,
31]. Эффективность препарата была
достоверно выше эффективности
плацебо (40% в сравнении с 20%). При
использовании терапевтических доз
(40-80 мг) выраженных
гемодинамических нарушений не
отмечалось. Наиболее частым
осложнением был ринит (у 21%
пациентов), изредка встречалиа
ловная боль, головокружение,
тахикардия. Прбтивв казанием к
назначению препарата являются арп
альная гипотония, ишемическая
болезнь сердца.
Абаноквил
Является высокоселективным
альфа-1 адреноблокатором (сродство к
альфа-1 рецепторам в 300 раз вы чем
к альфа-2). В качестве средства для
коррекций вводился внутрикавернозно
в малых дозах с хорошим эффектом у
пациентов с органической и
психогенной этиологией. Однако
местное действие продолжали менее 10
минут, что не позволяет широко
использовать абаноквил для лечения
ЭД [22, 38]. В настояЯ время
проводятся исследования оральной
формы пре парата в качестве
антиаритмика, однако данных об из
менении эректильной функции на фоне
ее приема"
Моксисилит
Новый селективный альфа-1
адреноблокатор. Со щается об
эффективности около 70% при внутри
вернозном введении в дозах 10-30 мг
[24,36]. В Евр( доступна оральная
форма препарата, однако чеп данных о
ее эффективности нет.
Доксазозин
В длительном (4 года)
исследовании селективв альфа-1
адреноблокатора доксазозина у
пациентов с пертонией и
доброкачественной гиперплазией про<
ты отмечено снижение частоты
эректильной дисфу ции по сравнению с
плацебо [27]. Все мужчи страдавшие
выраженной ЭД на момент начала исслс
вания, "выздоровели". Других данных,
подтверяод щих эффект препарата,
нет. Однако открываю хорошие
перспективы для использования
оральных лективных альфа-1
адреноблокаторов для лечения Э,
Агонисты допаминовых рецепторов
Апоморфин
Гйпоталамическая центральная
преоптическая на, богатая
допаминовыми рецепторами, является Е
ным интегративным центром,
участвующим в ВОЗЕ новении эрекции.
Кроме того, допаминэргическая
стимуляция активизирует
серотонинэргические зоны,
локализованные в срединной борозде,
что улучшает септо-гиппокампальную
холинергическую пере дачу, улучшая
эрекцию [19].
Апоморфин обладает прямым
действием на цент ральные Д2
рецепторы. Недавно была разработана
сублингвальная форма апоморфина,
которая показала ( эффективной у
многих пациентов с минимальной
кулогенной импотенцией [21]. В
другом исследован куда включались
пациенты с психогенной ЭД, эффект
отмечен у б7% [25]. Исследования III
фазы, проводящие ся в настоящее
время, должны показать эффективность
сублингвальной формы, назначаемой за
20-40 мин до коитуса у пациентов с
ЭД неопределенной органиче ской
этиологии.
Перспективы широкого
использования npenaта омрачаются его
побочными эффектами, включаю зевоту,
тошноту, рвоту, гипотензию.
Агонисты серотониновых
рецепторов
Тразодон
Известна тесная взаимосвязь между
парасимпап скими и серотониновыми
окончаниями в глад мышцах
кавернозных тел, т. о. последние
играют роль в регуляции
симпатического и парасимпатического
влияния. Тразодон является новым
антидепрессантом, не относящимся к
три- либо тетрациклическим.
Селективно ингибирует обратный
захват серотонина синапсами
головного мозга, кроме того,
блокирует альфа-адреноре-цепторы.
При использовании его для лечения
депрессий у 1:10000 развивался
приапизм, в связи с чем возлагаются
надежды на успешное применение его
при ЭД. Однако его эффективность у
60% пациентов была подтверждена лишь
в одном исследовании [26, 34].
Рекомендуемая доза 50-200 мг на
ночь. Побочные действия отмечаются
при применении высоких доз и
включают нарушение зрения, изменение
стула, тошноту, рвоту, сонливость,
дискоординацию, нарушения ритма
сердца и проводимости, гипотензию.
Доноры NO
L-аргинин
L-аргинин является
предшественником NO, и на него
возлагаются надежды по облегчению
натурального механизма эрекции [34,
37]. Однако в литературе имеются
данные лишь об одном
плацебо-контролируемом исследовании
с применением высоких доз L-аргинина
(2800 мг/сут). При применении в
течение 2 недель 40% пациентов
отметили улучшение эрекции [10].
Эффект был выше у молодых пациентов
с лучшими показателями кровотока.
Линсидомин
Донор NO для местного применения
представлен в 1992 г. Первые отчеты
сообщают об эфективности около 69%
при внутрикавернозном введении в
дозе 1 мг. При этом не наблюдалось
случаев приапизма и фиброзоподобных
изменений [28, 35].
Ингибиторы фосфодиэстеразы
Силденафил
NO, выделившийся из нервных и
эндотелиальных клеток в ответ на
сексуальный раздражитель,
стимулирует выработку ц-ГМФ в тканях
полового члена, что приводит к
снижению внутриклеточной
концентрации кальция и снижению
чувствительности сократительных
элементов к кальцию. Разрушение
ц-ГМФ до ГМФ происходит под
действием фосфодиэстеразы 5 типа
(ФДЭ5), фермента, специфичного для
кавернозной ткани.
Силденафил является селективным
ингибитором ФДЭ5. Т.о. препарат не
оказывает прямого действия на
гладкомышечные клетки, а усиливает
эффект NO и действует только в ответ
на сексуальную стимуляцию [6,19].
Появление силденафила открыло
новые перспективы оральной терапии
ЭД. Это первый препарат, который не
уступает в эффективности
внутрикавернозной терапии. Было
проведено более 20 двойных слепых,
плацебо контролируемых исследований
Виагры с участием более 3000 мужчин
с ЭД различной этиологии. Улучшение
эрекции отметили в среднем 78%
пациентов, развитие эрекции,
достаточной для проведения
пенетративного полового акта,
отметили более 75% пациентов.
Исследования, продолжавшиеся 12
месяцев, выявили сохранение эффекта
Виагры у 88% пациентов [2,4, б].
Препарат принимают за 60 минут до
сексуальной активности, период
полувыведения - 3-5 часов. На
чальная доза - 50 мг, в зависимости
от переносимости и эффективности
доза может быть снижена до 25.мг
либо повышена до максимальной, 100
мг. Максимальная частота приема - 1
раз в день. Препарат отличается
хорошей переносимостью. Побочные
явления включают головную боль (у
16% пациентов), приливы (10%),
диспепсию (7%), изменение зрения
(приобретение предметами голубого
оттенка, пелены перед глазами - у 3%
пациентов). Противопоказанием к
приему Виагры является прием любых
доноров азота или нитратов ввиду
резкого усиления их гипотензивного
действия. С осторожностью применяют
у пациентов с анатомической
деформацией полового члена, с
заболеваниями, предрасполагающими к
развитию приапизма
(серповидно-клеточная анемия,
множественная миелома, лейкоз), с
повышенной кровоточивостью, с
обострением язвенной болезни,
наследственным пигментным ретинитом.
Эта предосторожность вызвана
возможностью нарушения функции
тромбоцитов, т.к в них также
находится ФДЭ5.
Простагландин El (PGE1)
PGE1 активирует фермент
аденилатциклазу, которая
способствует превращению АТФ в
ц-АМФ, в результате чего происходит
гладкомышечное расслабление и
ту-менисценция.
С 1986 г. препараты PGE1 широко
применяются для диагностики и
лечения ЭД. По результатам
многочисленных исследований средняя
эффективность составляет 73% [3,
5,8].
Обычные дозы колеблются от 5 до
40 мкг. Тестирование начинают с 10
мкг, при необходимости постепенно
повышая дозу. При психогенной
эрекции начальная доза может быть
снижена до 5 мкг.
Наиболее частым побочным эффектом
является болезненная эрекция,
наблюдающаяся у 30% пациентов при
тестировании и у 15% при длительной
терапии препаратом. Такие серьезные
местные осложнения, как приапизм и
фиброзоподобные изменения,
встречаются редко (в 1 и 2,7%
случаев соответственно) [7].До
последнего времени препараты PGE1
были золотым стандартом
фармакотерапии ЭД.
Чтобы избежать таких неприятных
сторон внутрикавернозной терапии,
как необходимость самоинъекции и
болезненность, была разработана
трансуретральная система доставки
препарата MUSE. Несмотря на большее
удобство использования, система
имеет свои недостатки - раздражающее
действие препарата на слизистую
мочеиспускательного канала,
необходимость введения больших доз
препарата (125- 1000 мкг), что
делает терапию весьма дорогой. Кроме
того, у 10% партнерш после полового
акта отмечалось жжение во влагалище
и явления вагинита. Эффективность
внутриуретральной терапии ниже, чем
внутрикавернозной, около 66%
[21,24).
Нейротрансмиттеры
Кальцитонин ген-связанный пептид
(CGRP)
Этот пептид присутствует в
нервных окончаниях кавернозных тел.
Механизм действия заключается в
индукции аденилатциклазы, что
приводит к возрастанию концентрации
ц-АМФ. CGRP не индуцирует эрекцию
самостоятельно. По данным других
исследований, при совместном
введении с PGE1 развивалась эрекция
с высокой ригидностью. Сообщается,
что успех был достигнут у 30%
пациентов, не отвечавших на
монотерапию PGE1 [12,33].
Вазоинтестиналънъш пептид (VIP)
Полипептид также обнаружен в
кавернозной ткани. Механизм действия
сходен с таковым CGRP. По одним
данным, при его внутрикавернозном
введении туме-нисценция развивается,
но с недостаточной ригидностью.
Другими авторами сообщается, что при
совместном введении с фентоламином
эффект развивается почти у 100%
пациентов [29]. Эти данные
предварительны и требуют дальнейшего
исследования.
Гормональная терапия импотенции
Тестостерон
Терапия тестостероном показана
только в документированных случаях
гипогонадизма [13, 17, 22]. В
настоящее время пероральное
назначение считается менее
предпочтительным, чем
внутримышечное, из-за относительной
непредсказуемости плазменной
концентрации, возможности
токсического влияния на печень и
повышения уровня липидов сыворотки.
Применение трансдермального
тестостерона создает длительную,
ровную концентрацию препарата , но
иногда сопряжено с неудобством
нанесения (необходимостью выбривать
участок мошонки) [17,18, 33].
Бромокриптин
С успехом применяется только при
гипогонадизме, сочетанием с
гиперпролактинемией. Наиболее
полезен в лечении микроаденомы
гипофиза, приводящей к повышению
уровня пролактина сыворотки [14,
22].
Принципы комбинирования
лекарственных средств и группы
препаратов, применяемых для
сочетания
Комбинированная терапия ЭД еще не
получила широкого распространения,
но является перспективным
направлением, так как позволит:
- повысить эффективность
лечения
- снизить дозы
- уменьшить побочные эффекты
- подбирать терапию пациентам
с интеркуррентными
заболеваниями.
Эффект препаратов, влияющих на
эрекцию, реализуется по трем
основным путям (рис. З):
- Через гуанилат-циклазный
механизм (через него действуют
силденафил и доноры NO).
- Через аденилат-циклазный
механизм (посредством которого
действуют PGE1, CGRP, VIP).
- Через альфа-адренорецепторы
(действуют адреноблокаторы).
Синергизм лекарственных веществ
может быть обусловлен либо
суммированием действия по одному
пути активации эрекции, при этом
один препарат является
лекарством-помощником, либо
воздействием по разным путям с
усилением конечного результата.
В настоящее время хорошо изучены
и широко применяются лишь комбинации
вазоактивных препаратов для
интракавернозного введения:
папаверина, фентоламина и PGE1.
Папаверин и PGE1 действуют через
ц-АМФ, где папаверин является
лекарством-помощником, а фентоламин
действует через блокирование
альфа-адренорецепторов.
На данном примере достаточно
четко видно, что за счет комбинации
препаратов удается добиться
уменьшения побочных эффектов
(снижение частоты болезненных
эрекций с 15% до 2,4%, снижение
частоты развития пролонгированной
эрекции с 6,2% до 3,2% за счет
уменьшения дозировки), а также
урежения ускользания эффекта почти в
2 раза, что делает более удобным
применение комбинации длительное
время.
Предварительные данные о
применении комбинации фентоламина и
VIP говорят об эффективности
приближающейся к 100%. Это превышает
эффективность монотерапии этими
препаратами более чем в 2 раза.
Возможно, это обусловлено влиянием
на эрекцию по двум различным путям:
VIP- активирует аденилатциклазу,
фентоламин - блокирует
альфа-адренорецепторы.
Наглядно продемонстрирован
синергизм действия PGE1 и CGRP,
реализующийся через аденилатциклаз-'
ную систему, где CGRP выступает как
лекарство-помощник, усиливая
действие PGE1. Эффект комбинации
отмечен у 30% пациентов, не
отвечающих на другую
интракавернозную терапию. Данная
комбинация является примером
синергизма действия лекарственных
веществ по одному пути активации
эрекции, через ц-АМФ, с усилением
конечного результата.
В заключение настоящего обзора
нужно отметить, что у фармакотерапии
ЭД блестящее будущее. На протяжение
20 лет используются препараты PGE1
для интракавернозного применения,
считавшиеся золотым стандартом
консервативной терапии ЭД в 80-90-е
годы. С появлением силденафила
началась эра оральной фармакотерапии
ЭД. Однако ни PGE1, ни силденафил не
могут быть приемлемыми у всех
пациентов. Следующим шагом в
развитии фармакотерапии ЭД будет
создание комбинаций препаратов,
приближающее лечение к идеальному
для любого пациента. Литература
1. Грегуар А., Прайор Д. П.
Импотенция: интегрированный подход к
клинической практике. М., Медицина,
2000, с. 236.
2. Лоран О. Б., Аляев Ю. Г.,
Щеплев П. А. и др.
Виагра (силденафила цитрат) в
лечении больных с эректильной
дисфункцией // Урология, 2000, № 1,
с. 30- 33.
3. Ковалев В.А., Королева С. В.,
Комолое А, А.
Фармако-терапия эректильной
дисфункции // Урология, 2000, №1, с.
33-38.
4. Калиниченко С. Ю., Козлов Г.
И., Мельниченко Г. А, Дедов И. И.
Опыт применения силденафила цитрата
(виагры) у пациентов с сахарным
диабетом //Тер.
архив,1999,№10,с.78-80.
5. КоролеваС.В., КовалевВ.А,
КачаловАА,ЕфрелювЕ.А
Фармакотерапия эректильной
дисфункции. История. Современное
состояние проблемы // Андрология и
генитальная хирургия, 2000, №1, с.
113-114.
6. Viagra (sildenafil) и
эректильная дисфункция (руководство
для врачей). Pfizer, 1998, с. 25.
7. Штегман Б., Альбрехт Д. ПГЕ
1:
Прогресс в диагностике и терапии
эректильных дисфункций. 1995, с. 13.
8. Кротовский Г. С., Учкин И. Г.,
Забельская Т. Ф. и др,
Выбор метода лечения васкулогенной
эректильной дисфункции //
Андрология и генитальная хирургия,
2000, №1, с. 57-58.
9. BenetA E., MelmanA The
epidemiology of erectile
dis-function. Urol. Clin. North. Am.
1995; 22:699-709.
всего 41
наименований |